Controle biológico de Tetranychus urticae varia com temperatura
Uso combinado de Phytoseiulus persimilis e Amblyseius swirskii amplia controle em morangueiro
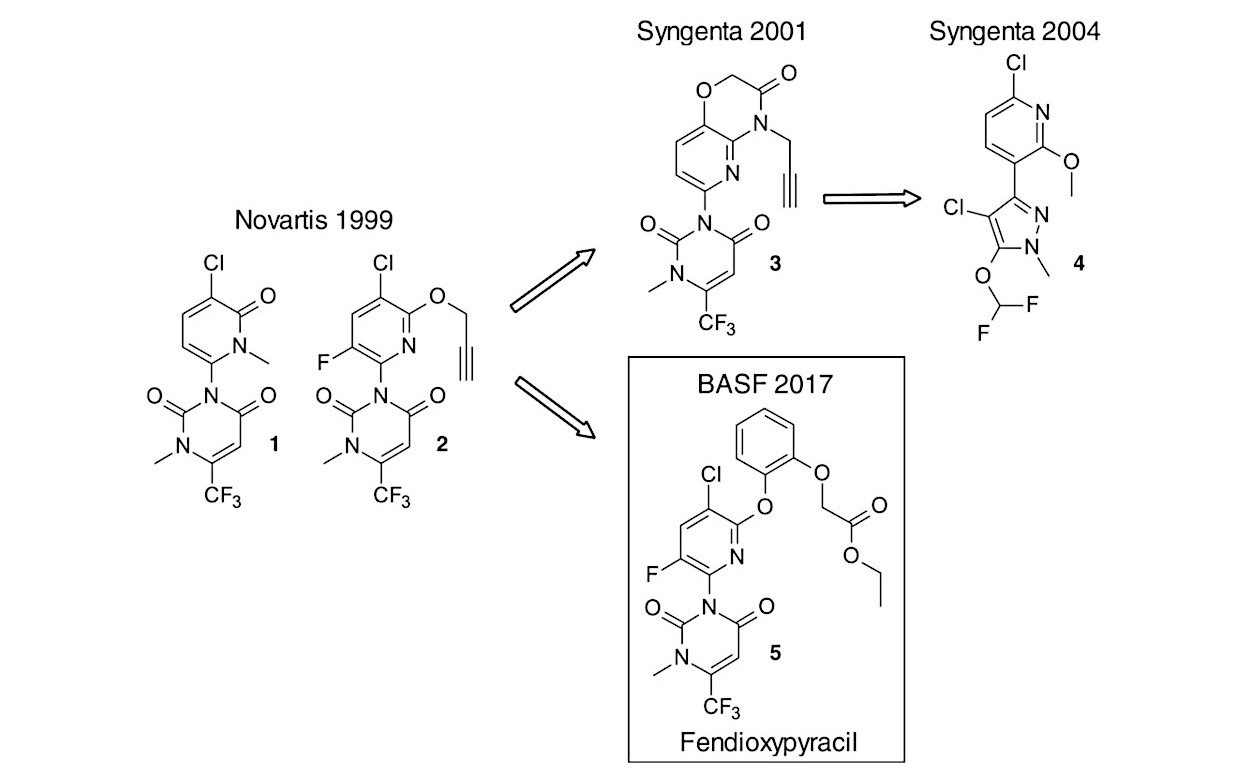
Um novo herbicida inibidor da protoporfirinogênio oxidase (PPO) surge como alternativa para manejo de plantas daninhas em pós-emergência. O fendioxypyracil apresenta atividade sistêmica e controle de amplo espectro em gramíneas e folhas largas, com alta eficácia em doses reduzidas.
O composto atua sobre enzimas PPO1 e PPO2, ligadas à biossíntese de clorofila e heme, explicam os cientistas envolvidos no projeto. A inibição bloqueia a conversão de protoporfirinogênio IX em protoporfirina IX. O acúmulo desse intermediário leva à formação de espécies reativas de oxigênio sob luz. O processo provoca dano de membranas, necrose e morte da planta.
Ensaios bioquímicos confirmaram o modo de ação. O fendioxypyracil apresentou valores de IC50 inferiores aos do padrão comercial saflufenacil para ambas as isoformas da enzima. O resultado indica maior potência, com destaque para PPO2 em Amaranthus tuberculatus.
Avaliações fisiológicas reforçaram o mecanismo. O herbicida induziu necrose rápida em tecidos expostos à luz e forte inibição de crescimento. A assimilação de CO2 caiu de forma expressiva. Não ocorreu inibição direta do fotossistema II, o efeito depende de luz. O perfil fisiológico alinhou o composto com outros inibidores PPO, com probabilidade superior a 99% para esse modo de ação.
Ensaios em casa de vegetação demonstraram amplo espectro. O produto controlou gramíneas como Avena fatua, Digitaria sanguinalis, Eleusine indica e Echinochloa crus-galli. O controle de folhas largas também ocorreu de forma consistente, explicam os pesquisadores envolvidos no projeto.
A eficácia apareceu em diferentes condições ambientais. Os experimentos incluíram casas de vegetação com temperaturas entre 12 ºC e 24 ºC. A avaliação visual indicou níveis elevados de dano às plantas daninhas poucos dias após aplicação.
A molécula combina núcleo de piridina com cadeia lateral ariloxílica. A estrutura favorece encaixe no sítio ativo da enzima. Essa configuração aumenta a atividade biológica e contribui para o desempenho em campo.
Mais informações em doi.org/10.1002/ps.70763

Receba por e-mail as últimas notícias sobre agricultura